OncoTalk: Neue, ermutigende Resultate für Frauen mit Brustkrebs
Neue, ermutigende Resultate für Frauen mit Brustkrebs, so der Titel des Novartis OncoTalks vom 2. April in Zürich. Prof. Dr. med. Jens Huober vom Kantonsspital St. Gallen hat die neusten, am San Antonio Breast Cancer Symposium 2008 vorgestellten Resultate der BIG-1-98 Studie zum Vergleich der Monotherapien und Sequenztherapien mit Letrozol bzw. Tamoxifen bei postmenopausalen Frauen mit Brustkrebs vorgestellt. Prof. Dr. med. Bernhard Pestalozzi vom Universitätsspital Zürich hat den aktuellen Informationsstand zur Antitumorwirkung des Bisphosphonats Zoledronat präsentiert.
 |
|
OncoTalk im Hotel Schweizerhof in Zürich | |
| |
Letrozol vs Tamoxifen in der adjuvanten Therapie bei postmenopausalen Frauen mit Brustkrebs
Über viele Jahre galt Tamoxifen als adjuvante Standardtherapie bei operierten Frauen mit Brustkrebs. Mit den Aromatasehemmern ist in der adjuvanten Brustkrebstherapie ein neues Zeitalter angebrochen.
Die BIG-1-98 Studie hat die Effektivität von Letrozol mit derjenigen von Tamoxifen verglichen. Sie erfolgte in zwei Phasen: Eine erste Kohorte, bestehend aus 1'828 postmenopausalen Frauen mit operablem, hormonrezeptorpositivem Brustkrebs, erhielt während 5 Jahren entweder Tamoxifen oder Letrozol als Monotherapie. In einer zweiten Kohorte mit 6'182 postmenopausalen Brustkrebspatientinnen wurden die Frauen nach einem von vier Therapieschemata adjuvant behandelt:
- Tamoxifen Monotherapie
- Letrozol Monotherapie
- Sequenztherapie Tamoxifen (2 Jahre) Letrozol (3 Jahre)
- Sequenztherapie Letrozol (2 Jahre) Tamoxifen (3 Jahre)
Primärer Studienendpunkt war das krankheitsfreie Überleben. Sekundäre Endpunkte waren Gesamtüberleben, fernmetastasenfreies Überleben und Nebenwirkungen.
Im Jahr 2005 wurden die ersten Resultate zum Vergleich der beiden Monotherapien publiziert [1]. Sie zeigten, dass 5 Jahre upfront Letrozol im Vergleich zu Tamoxifen das krankheitsfreie Überleben bei allen über 8'000 Frauen verbesserte und die Zeit bis zur Fernmetastasierung verlängerte.
Diese Resultate führten dazu, dass der Tamoxifen-Arm der BIG-1-98 Studie entblindet wurde, worauf rund ein Viertel der Patientinnen von Tamoxifen auf Letrozol wechselten. Diese Patientinnen wurden in der intention to treat Analyse weiter als Tamoxifen-Behandelte betrachtet und in einer zweiten, zensierten Analyse ausgeschlossen.
Monotherapie-Update
Am San Antonio Breast Cancer Symposium vom letzten Dezember präsentierten die Studienautoren die Monotherapieresultate nach einem mittleren Follow-up von 6 Jahren und 4 Monaten sowie die Sequenztherapieresultate versus Letrozol-Monotherapie [2].
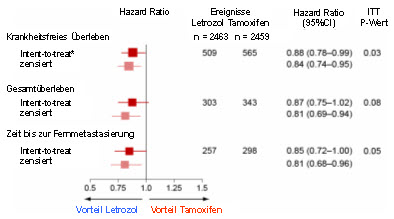
Abbildung 1 zeigt die Resultate des Monotherapievergleichs, jeweils in der intention to treat Analyse und der zensierten Analyse, also ohne Frauen, die von Tamoxifen auf Letrozol wechselten.
 |
|
Abbildung 1: Vergleich der Letrozol mit der Tamoxifen Monotherapie | |
| |
Das krankheitsfreie sowie das fernmetastasenfreie Überleben waren unter Letrozol in beiden Analysen signifikant besser. Die Gesamtmortalität war in der Letrozolgruppe um 13% (ITT-Analyse, p=0.08) respektive 19% (zensierte Analyse, deswegen ohne p-Wert-Angabe) geringer als in der Tamoxifengruppe. Die Überlegenheit von Letrozol war unabhängig vom Progesteronrezeptor- und HER2-Status, am ausgeprägtesten bei hoher Proliferationsaktivität (Ki67 hoch).
Vergleich Sequenztherapie Letrozol Monotherapie
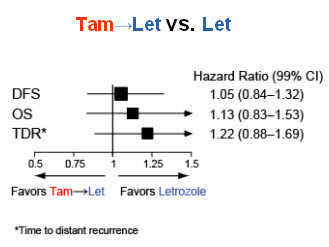
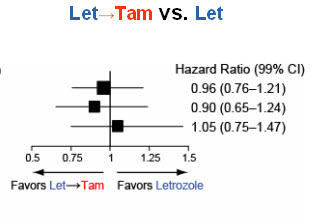
Der mittlere Follow-up für die Auswertung der Sequenztherapie versus Letrozol Monotherapie betrug knapp 6 Jahre. Die Resultate sind in Abbildung 2 illustriert.
|
|
|
Abbildung 2: Vergleich der beiden Sequenztherapien mit der Letrozol Monotherapie | |
| |
Zwischen den Therapieschemata Letrozol-Monotherapie und Letrozl gefolgt von Tamoxifen waren keine Unterschiede nachweisbar. Die Letrozol Monotherapie schien gegenüber Tamoxifen gefolgt von Letrozol leichte Vorteile zu zeigen, die Unterschiede im Überleben waren aber statistisch nicht signifikant. Weniger Brustkrebsereignisse unter Letrozol Monotherapie traten bei diesem Vergleich vor allem bei Frauen mit positivem Nodalstatus auf. Die Konklusion der Studienautoren aus diesen Resultaten: Die Sequenztherapie verbessert das Überleben im Vergleich zur Letrozol-Monotherapie nicht. Wird dennoch eine adjuvante Sequenztherapie erwogen, sollte mit Letrozol begonnen werden.
Prädiktoren für ein frühes Rezidiv in der BIG-1-98 Studie waren:
- Positiver LK-Status
- Progesteronrezeptor negativ
- Schlechte Differenzierung des Tumors
- HER2 Überexpression
- Tumorgrösse > 2 cm
- Vaskuläre Invasion
Implikationen für den klinischen Alltag Interview mit Prof. J. Huober
Prof. Huober, haben diese Studienresultate in der täglichen klinischen Praxis etwas verändert?
Ich glaube schon. Wir haben bereits in den letzten Jahren immer häufiger gerade Frauen mit einem hohen Rezidivrisiko upfront mit einem Aromatasehemmer behandelt. Diese Resultate geben uns nun die Bestätigung zu diesem Vorgehen.
Die Studienresultate zugunsten der Letrozol Monotherapie sind überzeugend; warum sollte man nach 2 Jahren auf Tamoxifen wechseln?
Es gibt Frauen, welche unter Letrozol zum Beispiel über stärkere Gelenkbeschwerden klagen; bei diesen Patientinnen sind wir froh, eine Alternative zu haben. Bei Frauen, welche mit dem Aromatasehemmer gut zurecht kommen, sehe ich keine Veranlassung, nach 2 Jahren auf Tamoxifen zu wechseln.
Sie sprechen Nebenwirkungen an. Wie sieht es denn mit dem Profil der beiden Substanzen aus?
Häufiger unter Aromatasehemmern beobachtete Nebenwirkungen sind Gelenkbeschwerden und Knochensubstanzverringerung. Tamoxifen seinerseits führt vermehrt zu klimakterischen Beschwerden; ausserdem sind unter Tamoxifen Eingriffe am Uterus und Endometriumkarzinome als auch thrombembolische Ereignisse häufiger.
Antitumorwirkung von Zoledronat
Ungefähr zwei Drittel aller Frauen mit einem Mammakarzinom erleiden im Verlauf ihrer Erkrankung eine pathologische Fraktur oder eine Wirbelsäulenkompression, bzw. müssen am Knochen operiert oder bestrahlt werden. Frauen mit einer pathologischen Fraktur haben eine signifikant schlechtere Überlebensprognose als solche ohne Frakturen. Bisphosphonate Zoledronat als Vertreter mit der grössen Effektivität in Bezug auf Reduktion von Skelettkomplikationen sind ein wichtiger Bestandteil der multimodalen Therapie von Knochenmetastasen. Tierversuche haben ausserdem gezeigt, dass Bisphosphonate eine günstige Wirkung auf die Entwicklung des Tumors haben könnten. Klinische Studien bestätigen diesen Effekt nun beim Menschen.
Überlebensvorteil bei prämenopausalen Frauen durch Zoledronat
An der 2009 im NEJM publizierten, randomisierten ABCSG-12 Studie nahmen 1803 prämenopausale Frauen mit Hormonrezeptor-positivem, früh diagnostiziertem Brustkrebs teil [3]. Die Behandlung bestand in einer postoperativen Behandlung mit Goserelin/Tamoxifen respektive Goserelin/Anastrozol mit oder ohne 4 mg intravenösem Zoledronat alle halbe Jahre für insgesamt 3 Jahre. Primärer Endpunkt war das krankheitsfreie Überleben.
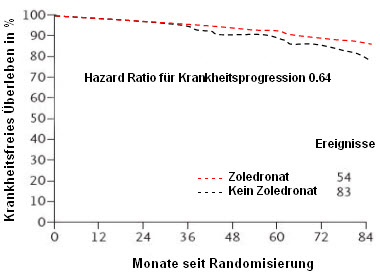
Der Unterschied im krankheitsfreien Überleben zwischen der Anastrozolgruppe und der Tamoxifengruppe war nicht signifikant. Hingegen profitierten die Patientinnen signifikant von Zoledronat: die relative Risikoreduktion für ein krankheitsassoziiertes Ereignis betrug 36% (p=0.01), einer absoluten Risikoreduktion von 3.2% entsprechend (siehe Abbildung 3).
 |
|
Abbildung 3: Krankheitsfreies Überleben mit und ohne Zoledronat | |
| |
Die Verträglichkeit der Behandlung mit Zoledronat in Kombination mit der endokrinen Therapie war gut (wenig Grad 3 und 4 Nebenwirkungen, keine Nierentoxizität).
Viel versprechende Resultate auch bei postmenopausalen Frauen
In der ZO-FAST Studie erhielten 1'064 postmenopausale Patientinnen mit Hormonrezeptor-positivem, früh diagnostiziertem Mammakarzinom zu täglich 2.5 mg Letrozol das Bisphosphonat Zoledronat alle 6 Monate, und zwar je nach Randomisierung entweder upfront oder erst beim Auftreten einer pathologischen Fraktur oder einem T-Score in der Knochendensitometrie von < 2.0 [4]. Endpunkte waren die Knochendichteveränderungen in der LWS nach einem Jahr (primärer Endpunkt), krankheitsfreies Überleben, Gesamtüberleben, Frakturrate und Sicherheit.
Die am San Antonio Breast Cancer Symposium von Antonio vorgestellten Follow-up Resultate nach 3 Jahren zeigten, dass die Knochendichte unter sofort verabreichtem Zoledronat zunahm und unter verzögert verabreichtem Zoledronat abnahm. Die Unterschiede waren hoch signifikant. Überraschend gross war der Unterschied zwischen den Gruppen auch beim krankheitsfreien Überleben; die relative Risikoreduktion bei initial verabreichtem gegenüber verzögert verabreichtem Zoledronat betrug 40% (HR 0.585, p=0.03). Die Therapie wurde gut vertragen.
Erste positive Resultate im neoadjuvanten Setting
Eine Subgruppenanalyse der AZURE Studie untersuchte den Effekt von 4 mg Zoledronsäure bei 205 Brustkrebspatientinnen in Kombination mit einer neoadjuvanten Chemotherapie (Anthrazykline/Taxane) [5]. Primärer Endpunkt war die Tumorgrösse, welche zum Zeitpunkt der Operation zurückblieb.
Die Grösse des Residualtumors war bei den Frauen, welche Zoledronsäure zur Chemotherapie bekamen, um 33% geringer als bei den Frauen ohne Zoledronat (p=0.002). Eine pathologische komplette Remission trat bei neoadjuvant mit Zoledronat behandelten Frauen signifikant häufiger auf (+88%, p=0.033).
Implikationen für den klinischen Alltag Interview mit Prof. B. Pestalozzi
Prof. Pestalozzi, welchen Frauen ist denn gemäss der aktuellen Datenlage konkret Zoledronat zu empfehlen?
Für generelle Empfehlungen ist es noch zu früh. An der Konsensuskonferenz von St. Gallen wurde die Frage gestellt, ob man knochengesunden Brustkrebspatientinnen in der adjuvanten Situation Zoledronat empfehlen soll oder nicht. Bei den prämenopausalen Frauen war die Antwort zu etwa 40% und bei den postemnopausalen Frauen zu etwa 20% ja. Der Entscheid, ob einer Frau nach Entfernung des Tumors zusätzlich zur adjuvanten Systemtherapie noch Zoledronat verschrieben wird, muss heute individuell erfolgen, unter Berücksichtigung der Knochendichte. Wenn wir die vollständigen Resultate der AZURE-Studie mit über 3'000 Patientinnen dann kennen, können wir hoffentlich mehr sagen.
Werden Sie von den Frauen in Ihrer Praxis auf die Antitumorwirkung von Zoledronat angesprochen?
Ja. Es gibt natürlich immer mehr Frauen, die sich im Internet über neuste Studienresultate informieren. Auch der Wunsch der Patientin ist ein relevanter Faktor für jeden Therapieentscheid.
Gibt es andere Bisphosphonate mit Antitumorwirkung?
2006 wurde in einer kleineren Studie für Clodronat ein orales Bisphosphonat eine Antitumorwirkung gezeigt. Die Resultate haben aber wenig Echo ausgelöst, wohl weil die oralen Bisphosphonate eine Reihe von Nachteilen haben; insbesondere die unregelmässige Absorption, die Notwendigkeit der nüchternen Einnahme und die viel häufigere Einnahmefrequenz als bei Zoledronat.
Wird Zoledronat auch bei anderen Knochenmetastasen eingesetzt?
Am Anfang hat man gemeint, es wirke nur bei osteolytischen Knochenmetastasen, was sich nicht bewahrheitet hat. Heute ist Zoledronat einmal monatlich verabreicht - für die Erhaltung der Knochenstruktur bei Metastasen aller soliden Tumoren zugelassen.
Referenzen
1. Thürlimann B et al for the Breast International Group (BIG) 1-98 Collaborative Group. A comparison of letrozole and tamoxifen in postmenopausal women with early breast cancer. N Engl J Med 2005;353:2747-2757
2. Mouridsen H for the BIG 1-98 Collaborative Group. BIG 1-98: A randomized double-blind phase III study evaluating letrozole and tamoxifen given in sequence as adjuvant therapy for postemnopausal women with receptor-positive breast cancer. San Antonio Breast Cancer Symposium 2008, Abstract 13
3. Gnant M et al. Endocrine therapy plus zoledronic acid in premenopausal breast cancer. N Engl J Med 2009;360:679-691
4. Eidtmann H et al. The effect of zoledronic acid on aromatase inhibitor associated bone loss in postmenopausal women with early breast cancer receiving adjuvant letrozole: 36 months follow-up of ZO-FAST. San Antonio Breast Cancer Symposium 2008, Abstract 44
5. Winte MC et al. The addition of zoledronic acid to neoadjuvant chemotherapy may influence pathological response - exploratory evidence for direct anti-tumor activity in breast cancer. San Antonio Breast Cancer Symposium 2008, Abstract 5101
Mediscope
23.04.2009 - dde
Mit freundlicher Unterstützung von Novartis